Le vasche per uccelli sono utili per aiutare gli uccelli a mantenersi idratati quando è difficile trovare acqua potabile, ad esempio durante le estati calde o gli inverni freddi. Possono essere dotate di elementi riscaldanti per impedirne il congelamento in inverno. Ma questo è utile solo con temperature sotto lo zero... o forse no?
Un esempio viene dalla "scienza" delle vasche per uccelli. È stato osservato che nei giorni in cui la temperatura esterna non è mai scesa sotto i 4 °C, la superficie dell'acqua si congelava comunque, lasciando gli uccelli non solo al freddo, ma anche assetati. Sorprendentemente, la domanda su come l'acqua possa congelare al di sopra della sua temperatura di fusione può essere risolta spiegando come possa evaporare al di sotto del suo punto di ebollizione, due fenomeni apparentemente non correlati.
Evaporazione al di sotto dei 100°C
In un precedente articolo abbiamo parlato dell'acqua come uno dei più potenti refrigeranti in natura. Tra tutti i liquidi, infatti, possiede il più alto calore latente di vaporizzazione, il che significa che serve più energia che per qualsiasi altro liquido per rompere i legami tra le molecole e trasformare l’acqua in vapore acqueo.
Mentre sono necessari solo 4,2 kJ di calore per aumentare la temperatura di un litro d'acqua di un grado (diciamo da 99 °C a 100 °C, il suo ben noto punto di ebollizione a livello del mare), per far evaporare la stessa quantità d'acqua è necessaria una quantità di calore oltre 500 volte superiore: 2256 kJ/kg!
Ma ciò che molti non sanno è che non è necessario portare l'acqua a ebollizione per trasformarla in vapore. Semplicemente, l’acqua sembra comportarsi come se non avesse altra scelta se non evaporare quando raggiunge i 100 °C. In realtà può evaporare perfettamente anche a temperature molto più basse, purché venga messa nelle condizioni di farlo.
E questo ha perfettamente senso: se si stende il bucato appena lavato, si asciugherà in un paio di giorni. Allo stesso modo, IntrCooll e PreCooll di Oxycom sfruttano il principio dell'evaporazione per raffreddare l'aria; in nessuno dei due casi l'acqua coinvolta deve essere riscaldata fino a 100 °C.
Come l'umidità influenza l'evaporazione
La domanda è quindi: come si fa a forzare l'evaporazione dell'acqua già a temperatura ambiente? È abbastanza semplice: sfruttando il fatto che la natura non sembra amare i cambiamenti bruschi, un po’ come accade anche negli esseri umani.
L’acqua, in forma liquida, è composta da molecole d’acqua molto fitte, che però sono ancora libere di muoversi. L’aria, invece, è un gas costituito principalmente da molecole di azoto e ossigeno in rapido movimento, oltre a una piccola percentuale di altre molecole come argon e anidride carbonica; questa miscela è chiamata aria secca. Può contenere anche una piccola quantità di vapore acqueo, tipicamente intorno all’1%; la miscela di aria secca e vapore acqueo è chiamata aria umida.
Si può quindi pensare all’acqua come a “tante molecole d’acqua” e all’aria umida come a “pochissime molecole d’acqua”.
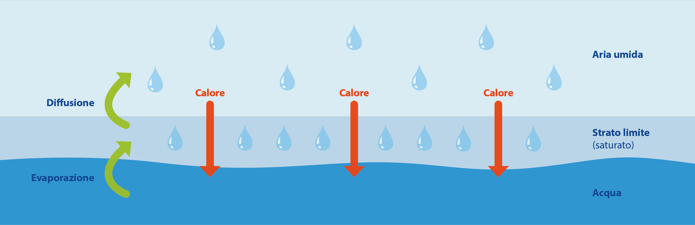
Quando l’acqua è esposta all’aria, si crea una transizione molto netta tra la zona ricca di molecole d’acqua e quella povera di molecole d’acqua. Questa discontinuità, poco “gradita” dalla natura, viene attenuata dalla formazione di uno strato limite intermedio. Questo strato limite è ancora aria umida, ma è ora completamente satura, cioè contiene la massima concentrazione possibile di vapore acqueo a una determinata temperatura.
Può essere visto come una sorta di media tra lo strato di acqua liquida e l'aria umida insatura circostante, che contribuisce a tranquillizzare, per così dire, gli equilibri della natura.
Diffusione e flusso d’aria
A questo punto entra in gioco un altro importante fenomeno naturale. Proprio come gli oggetti cadono sempre verso il basso, o come i cavi tendono sempre ad aggrovigliarsi ma non a districarsi da soli, anche il vapore acqueo tende a muoversi da zone a concentrazione più alta (lo strato limite) verso zone a concentrazione più bassa (l’aria umida circostante): questo processo è chiamato diffusione.
La diffusione avviene spontaneamente, ma può essere accelerata notevolmente utilizzando un ventilatore che forza il flusso d’aria sopra la superficie dell’acqua.
Il risultato è che l’aria diventa più umida, ma al tempo stesso lo strato limite si impoverisce di vapore acqueo. A questo punto la natura reagisce nuovamente trasformando l’acqua in vapore per ristabilire lo stato iniziale di saturazione dello strato limite. Tuttavia, bisogna ricordare che questa trasformazione richiede molta energia, che viene sottratta all’aria stessa.
Di conseguenza, l’aria non solo diventa più umida, ma si raffredda.
Umidità e calo di temperatura
Questo processo avviene sia a temperatura ambiente, sia in prossimità del punto di congelamento dell’acqua, sia a temperature più vicine al punto di ebollizione: in altre parole, può verificarsi a qualsiasi temperatura. È addirittura più efficiente a temperatura ambiente che al punto di ebollizione, grazie al più elevato calore latente di vaporizzazione: 2454 kJ/kg a 20 °C.
Ciò significa che per ogni aumento di 1 g/kg dell’umidità assoluta causato dall’evaporazione forzata, la temperatura diminuisce di circa 2,5 °C.
Questo processo continua fino a quando l'aria non è completamente satura e non può più contenere acqua. La temperatura che l'aria ha raggiunto a quel punto è chiamata temperatura di bulbo umido, ovvero la temperatura più bassa possibile grazie all'evaporazione.
A tal proposito, il sistema IntrCooll utilizza una tecnica intelligente per “ingannare” la natura e raffreddare l’aria fino a temperature inferiori al bulbo umido, ma questa è forse una storia per un’altra volta.
Capire la temperatura di bulbo umido
Il termine temperatura di bulbo umido potrebbe non essere familiare a tutti, ma può essere interpretato in modo letterale.
Un termometro tradizionale a liquido in vetro ha un bulbo alla base riempito di alcol, che si espande quando la temperatura aumenta. La lettura del termometro è ciò che chiamiamo temperatura, ma in senso stretto si tratta della temperatura di bulbo secco.
Se copriamo questo bulbo con un panno imbevuto d’acqua (il “bulbo umido”) e, per favorire il processo, facciamo circolare dell’aria attorno ad esso, il termometro mostrerà un valore più basso: la temperatura di bulbo umido.
In modo inconscio, tutti abbiamo familiarità con questo fenomeno: per esempio, uscendo dalla doccia o da una piscina, si avverte improvvisamente una sensazione di freddo più intensa: l’evaporazione indotta sottrae calore alla pelle e ciò che si percepisce è, di fatto, la temperatura di bulbo umido.
Tuttavia, a differenza della temperatura apparente (che è la temperatura percepita dagli esseri umani, basata sul fattore di raffreddamento del vento e quindi soggettiva per definizione), la temperatura di bulbo umido è una grandezza fisica reale, misurabile in modo oggettivo.
Perché una vasca per uccelli si congela sopra gli zero gradi
Ora siamo pronti a tornare all'esempio della vasca per uccelli.
È emerso che, anche se la temperatura di bulbo secco registrata durante l’intera giornata era rimasta sopra 0 °C, quindi costantemente al di sopra del punto di congelamento, è stata la temperatura di bulbo umido all’interfaccia acqua/aria a scendere sotto lo zero, causando il congelamento della vasca.
In altre parole, l’evaporazione continua può sottrarre così tanto calore dalla superficie dell’acqua da portare localmente la temperatura sotto il punto di congelamento, anche se l’aria circostante resta sopra zero.
Uccelli ancora assetati, purtroppo — ma la rispsota della scienza è davvero affascinante.

/Case%20studies%20(Pictures)/VCN/Oxycom%20-%20Clauger.jpg?width=900&height=900&name=Oxycom%20-%20Clauger.jpg)
/Case%20studies%20(Pictures)/Equinix/PreCooll%20adiabatisch.jpg?width=1400&height=1050&name=PreCooll%20adiabatisch.jpg)


/BMI%20adiabatic%20cooling.jpeg?width=400&name=BMI%20adiabatic%20cooling.jpeg)
.png?width=400&name=VDI%206022%20(met%20witruimte).png)
